A história da vida aeróbia pode ser compreendida como uma negociação contínua com o oxigênio. A transição da Terra primitiva, marcada por uma atmosfera redutora, para um ambiente progressivamente oxidante, culminando no Grande Evento de Oxigenação, impôs um desafio químico sem precedentes às formas de vida ancestrais. O oxigênio molecular (O₂), apesar de representar o aceitador final de elétrons mais eficiente da bioenergética conhecida, apresenta uma estrutura eletrônica singular: trata-se de um birradical, contendo dois elétrons desemparelhados em seus orbitais externos.
Elétrons vivem em “nuvens” chamadas orbitais. Quando dois oxigênios se unem, essas nuvens se reorganizam. No final, sobram dois elétrons sozinhos em orbitais diferentes. Por isso, o oxigênio é um birradical, mesmo sendo estável o suficiente para sustentar a vida. Essa característica confere ao oxigênio uma reatividade latente, que se manifesta sempre que sua redução ocorre de maneira incompleta. Assim, a própria base da vida aeróbia carrega um paradoxo fundamental: a dependência absoluta de um agente cuja química favorece a geração de espécies potencialmente tóxicas.

Do ponto de vista estritamente químico, a redução do oxigênio pode seguir caminhos distintos. Na mitocôndria, a citocromo c oxidase catalisa a transferência concertada de quatro elétrons ao O₂, promovendo sua redução direta a água, reação energeticamente eficiente e biologicamente segura. Contudo, em ambientes celulares ricos em equivalentes redutores, como NADH e FADH₂, a redução do oxigênio frequentemente ocorre de forma univalente, isto é, pela transferência sequencial de elétrons individuais. A primeira dessas etapas gera o ânion superóxido (O₂•⁻), uma espécie relativamente pouco reativa, mas de enorme relevância biológica. O superóxido pode sofrer dismutação espontânea ou catalisada por superóxido dismutases, produzindo peróxido de hidrogênio (H₂O₂), uma molécula não radical, porém quimicamente ativa. Em presença de íons metálicos redox-ativos, como ferro ou cobre, o H₂O₂ pode ainda ser convertido em radical hidroxila (•OH) por meio da reação de Fenton. Este último representa uma das espécies químicas mais reativas conhecidas em sistemas biológicos, capaz de oxidar lipídios, proteínas e ácidos nucleicos de maneira difusional e praticamente indiscriminada.
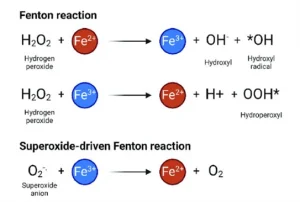
A toxicidade associada às espécies reativas de oxigênio, portanto, não deriva apenas de sua formação, mas da interação entre essas espécies e o contexto químico celular, em especial a disponibilidade de metais de transição. Ferro e cobre ilustram de forma exemplar essa ambiguidade. Ambos são essenciais à vida, integrando centros catalíticos de enzimas, proteínas de transporte eletrônico e sistemas de sinalização. Entretanto, quando liberados de seus sítios proteicos ou presentes em excesso no compartimento celular inadequado, tornam-se catalisadores eficientes da geração de radicais hidroxila. A homeostase metálica, assegurada por proteínas como ferritina, transferrina e metalotioneínas, emerge assim como um componente central da defesa antioxidante. Em contraste, metais redox-inertes, como cádmio e arsênio, exercem seus efeitos deletérios de forma indireta, ao se ligarem a grupos sulfidrila, inibirem enzimas antioxidantes e promoverem depleção de glutationa, desorganizando o equilíbrio redox sem participar diretamente de reações de oxirredução.
A evolução da vida aeróbia foi acompanhada pelo refinamento progressivo de sistemas antioxidantes. Moléculas de baixo peso molecular, como a glutationa reduzida, o ácido ascórbico e os tocoferóis, funcionam como tampões redox, capazes de doar elétrons e neutralizar espécies reativas. Em paralelo, sistemas enzimáticos altamente especializados, como superóxido dismutases, catalase e glutationa peroxidases, promovem a conversão controlada de espécies reativas em produtos menos agressivos. Contudo, a biologia redox contemporânea ultrapassa a noção de defesa passiva. O peróxido de hidrogênio, em particular, passou a ser reconhecido como um mensageiro intracelular legítimo. Em concentrações finamente reguladas e em microdomínios específicos, o H₂O₂ oxida seletivamente resíduos de cisteína em proteínas regulatórias, modulando a atividade de quinases, fosfatases e fatores de transcrição. O estresse oxidativo, nessa perspectiva, não se define pela simples presença de oxidação, mas pela perda de controle espacial, temporal e quantitativo dessas reações.
Essa ambivalência funcional das espécies reativas torna-se especialmente evidente no contexto do exercício físico. A contração muscular eleva abruptamente a demanda energética, aumentando o fluxo de elétrons na cadeia respiratória mitocondrial e ativando sistemas produtores de espécies reativas, como NADPH oxidases, xantina oxidase e vias associadas ao metabolismo de catecolaminas. Durante muito tempo, esse aumento transitório de espécies reativas foi interpretado exclusivamente como um fenômeno deletério, associado à fadiga, à inflamação e à lesão muscular. Evidências mais recentes, contudo, demonstram que a produção aguda e controlada de espécies reativas constitui um sinal essencial para a adaptação ao treinamento, especialmente no exercício de endurance.

He F, Li J, Liu Z, Chuang CC, Yang W, Zuo L. Redox Mechanism of Reactive Oxygen Species in Exercise. Front Physiol. 2016 Nov 7;7:486.
O peróxido de hidrogênio gerado durante o exercício atua como elo químico entre o aumento do fluxo metabólico e a reprogramação celular de longo prazo. Por meio da oxidação reversível de cisteínas sensíveis, o H₂O₂ ativa vias de sinalização que culminam na indução de coativadores transcricionais, como o PGC-1α, considerado regulador central da biogênese mitocondrial. A ativação dessa via promove aumento da densidade mitocondrial, elevação da capacidade oxidativa e fortalecimento dos sistemas antioxidantes endógenos. Esse processo ilustra um princípio hormético fundamental: exposições repetidas a estímulos oxidantes moderados induzem adaptações que aumentam a resiliência redox do músculo esquelético.
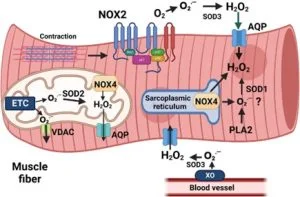
Powers SK, Radak Z, Ji LL, Jackson M. Reactive oxygen species promote endurance exercise-induced adaptations in skeletal muscles. J Sport Health Sci. 2024;13(6):780-792.
Paradoxalmente, estados celulares altamente redutores também podem favorecer a geração de espécies reativas. Em condições de estresse redutivo, caracterizadas por razões elevadas de NADH/NAD⁺ ou NADPH/NADP⁺, o excesso de elétrons pode ser transferido diretamente ao oxigênio por flavoproteínas mitocondriais, como glutationa redutase e tiorredoxina redutase, resultando na formação de peróxido de hidrogênio. Esse fenômeno demonstra que tanto a oxidação excessiva quanto a redução extrema perturbam a homeostase redox, reforçando a noção de que existe um intervalo ótimo de equilíbrio químico no qual a sinalização redox é funcional e o dano é minimizado.
No campo da imunologia, a produção deliberada de espécies reativas por neutrófilos e macrófagos exemplifica de forma paradigmática essa dualidade. O burst respiratório, mediado pela ativação de NADPH oxidase, gera superóxido e seus derivados como mecanismo de defesa antimicrobiana. Embora eficaz contra patógenos, esse processo pode causar dano colateral ao tecido hospedeiro, sendo a inflamação o preço fisiológico de um sistema imune altamente responsivo. Enzimas antioxidantes atuam, nesse contexto, como moduladores finos da resposta inflamatória, limitando a extensão e a duração do dano oxidativo.
A avaliação do estresse oxidativo em humanos acrescenta uma dimensão metodológica relevante a essa discussão. Devido à curta meia-vida e à alta reatividade das espécies reativas, sua mensuração direta é extremamente difícil. Assim, a pesquisa recorre a biomarcadores indiretos de oxidação de lipídios, proteínas e DNA, bem como à análise da capacidade antioxidante total. Revisões sistemáticas em atletas e corredores demonstram que não existe um marcador universal de estresse oxidativo induzido pelo exercício. O perfil observado depende do estado de treinamento, da intensidade e duração do esforço e do momento da coleta, reforçando a ideia de que o estresse oxidativo é um fenômeno dinâmico e contextual.
Nesse cenário, a suplementação antioxidante exógena surge como tema de debate. Embora antioxidantes possam atenuar marcadores de oxidação aguda, evidências crescentes indicam que a suplementação crônica, especialmente em doses elevadas de vitaminas antioxidantes clássicas, pode interferir negativamente nas adaptações ao treinamento. Ao amortecer excessivamente os sinais redox, tais intervenções podem reduzir a ativação de vias dependentes de espécies reativas, comprometendo ganhos em biogênese mitocondrial e na indução de defesas antioxidantes endógenas. Assim, a literatura converge para uma visão cautelosa: no contexto adaptativo, nem toda redução do estresse oxidativo é desejável.
Do ponto de vista evolutivo, a capacidade de conviver com espécies reativas foi decisiva para a complexificação da vida. Cianobactérias ancestrais, primeiras a produzir oxigênio intracelularmente, provavelmente sobreviveram ao desafio oxidativo por meio da exaptação de sistemas redutores pré-existentes com propriedades antioxidantes fortuitas, antes da evolução de defesas enzimáticas especializadas. A precipitação oxidativa do ferro ambiental, ao reduzir sua biodisponibilidade, representou simultaneamente um desafio nutricional e uma vantagem protetora contra reações de Fenton descontroladas. A história da vida aeróbia, portanto, não é a história da eliminação do estresse oxidativo, mas da sua integração funcional à bioenergética, à sinalização e à adaptação.
Em síntese, a integração das evidências aqui discutidas sustenta uma visão unificada da biologia redox como eixo organizador da fisiologia moderna. Espécies reativas de oxigênio, metais de transição e sistemas antioxidantes constituem uma rede química interdependente que conecta metabolismo energético, sinalização celular e adaptação ao exercício. O estresse oxidativo emerge quando essa rede perde coerência regulatória, seja por excesso, deficiência ou deslocalização das reações redox. No exercício, na evolução e na doença, a fronteira entre toxicidade e sinalização não é definida pela presença das espécies reativas em si, mas pela arquitetura molecular que governa seu uso.
REFERÊNCIAS
DAVIES, K. J. A. Oxidative stress: the paradox of aerobic life. Biochemical Society Symposium, v. 61, p. 1–31, 1995.
FISCHER, W. W.; HEMP, J.; VALENTINE, J. S. How did life survive Earth’s great oxygenation? Current Opinion in Chemical Biology, v. 31, p. 166–178, 2016.
GOMES, E. C.; SILVA, A. N.; OLIVEIRA, M. R. Oxidants, antioxidants, and the beneficial roles of exercise-induced production of reactive species. Oxidative Medicine and Cellular Longevity, v. 2012, Article ID 756132, 2012.
GUPTA, R. R.; GUPTA, M.; BHICKTA, S. Reactive oxygen species (ROS): a review. Dental Journal of Advance Studies, v. 1, n. 3, p. 152–158, 2013.
GUTTERIDGE, J. M. C.; HALLIWELL, B. Oxidative stress, redox stress or redox success? Biochemical and Biophysical Research Communications, v. 502, p. 183–186, 2018.
HALLIWELL, B. Reactive species and antioxidants: redox biology is a fundamental theme of aerobic life. Plant Physiology, v. 141, p. 312–322, 2006.
KORGE, P.; CALMETTES, G.; WEISS, J. N. Increased reactive oxygen species production during reductive stress. Biochimica et Biophysica Acta, v. 1847, p. 514–525, 2015.
MASON, S. A. et al. Antioxidant supplements and endurance exercise: current evidence and mechanistic insights. Redox Biology, v. 35, 101471, 2020.
POWERS, S. K. et al. Exercise-induced oxidative stress: friend or foe? Journal of Sport and Health Science, v. 9, p. 415–425, 2020.
POWERS, S. K. et al. Reactive oxygen species promote endurance exercise-induced adaptations in skeletal muscles. Journal of Sport and Health Science, v. 13, p. 780–792, 2024.
RAHAL, A. et al. Oxidative stress, prooxidants, and antioxidants: the interplay. BioMed Research International, v. 2014, Article ID 761264, 2014.
THIRUPATHI, A. et al. Effect of running exercise on oxidative stress biomarkers: a systematic review. Frontiers in Physiology, v. 11, 610112, 2021.
VALKO, M. et al. Redox- and non-redox-metal-induced formation of free radicals and their role in human disease. Archives of Toxicology, v. 90, p. 1–37, 2016.
