O treinamento de endurance impõe ao organismo um conjunto de estímulos fisiológicos — hemodinâmicos, metabólicos, mecânicos e hormonais — que atuam de forma integrada para ampliar a capacidade de transporte e utilização de oxigênio. A literatura clássica em fisiologia do exercício mostra que essas adaptações começam no sangue e se propagam por todo o sistema cardiorrespiratório, sendo a expansão da volemia, as alterações no hematócrito e a modulação da eritropoiese elementos centrais dessa resposta orgânica.
O aumento da volemia é uma das adaptações mais precoces e consistentes observadas com o início de programas de endurance. A combinação de repetidos episódios de aumento do fluxo sanguíneo, elevação da temperatura corporal, ativação simpática e liberação de peptídeos natriuréticos cria um ambiente favorável à expansão do volume plasmático. Mecanismos como retenção renal de água e sódio, aumento da síntese hepática de proteínas plasmáticas (particularmente albumina) e maior expressão de transportadores osmóticos nas células endoteliais promovem uma rápida hemodiluição inicial. Essa expansão do plasma reduz a viscosidade sanguínea, melhora o retorno venoso e facilita o aumento do volume sistólico — ajustes considerados essenciais para sustentar maiores débitos cardíacos durante o exercício prolongado.
Como consequência, o hematócrito frequentemente diminui nas primeiras semanas de treinamento, não por perda de hemácias, mas por diluição relativa. Essa queda, longe de indicar prejuízo funcional, faz parte de um processo adaptativo que otimiza o fluxo sanguíneo e reduz o custo energético do trabalho cardíaco. Com a continuidade do treinamento e o aumento da demanda metabólica dos tecidos ativos, o organismo tende a reequilibrar essa relação: o volume plasmático permanece expandido, mas passa a ser acompanhado por aumento gradual da massa de glóbulos vermelhos (Hbmass), modulando novamente o hematócrito em direção a valores compatíveis com maior capacidade de transporte de oxigênio.
O estímulo à eritropoiese resulta da conjunção de fatores regulatórios que incluem hipóxia relativa dos tecidos durante esforços prolongados, maior gradiente arteriovenoso de oxigênio, microtrauma eritrocitário induzido por estresse mecânico e aumento do fluxo sanguíneo pulsátil nos capilares da medula óssea. Episódios repetidos de hipóxia funcional — mesmo em condições normóxicas — ativam de forma incremental os fatores induzíveis por hipóxia (HIFs), promovendo maior sensibilidade das células peritubulares renais à redução transitória da pressão parcial de oxigênio e, consequentemente, estimulando a liberação de eritropoietina (EPO). A EPO, por sua vez, acelera a maturação dos precursores eritroides e aumenta a taxa de produção de reticulócitos, aumentando progressivamente o número de hemácias circulantes.
Além disso, o treinamento de endurance aumenta o estresse mecânico sobre a coluna de glóbulos vermelhos, especialmente em modalidades como corrida e ciclismo de longa duração, favorecendo a hemólise intravascular fisiológica e, paradoxalmente, contribuindo para sinalizar a necessidade de reposição por via eritropoiética. Esse processo, acoplado ao aumento da demanda metabólica muscular, cria um ciclo de feedback positivo no qual estímulos hemodinâmicos, metabólicos e mecânicos convergem para ampliar a massa eritrocitária.
Assim, o sangue responde ao treinamento de endurance como um tecido altamente plástico, modulando sua composição para garantir eficiência no transporte de oxigênio e na regulação térmica, ao mesmo tempo em que reduz o custo hemodinâmico associado ao trabalho cardíaco. Essas adaptações não são meramente acessórios fisiológicos do treinamento, mas sim um passo fundamental no desenvolvimento de maior capacidade aeróbia, influenciando diretamente o VO₂máx e a performance em atividades prolongadas. A interação entre expansão plasmática, ajustes no hematócrito e aumento da eritropoiese constitui, portanto, uma das expressões mais claras do princípio da sobrecarga progressiva aplicado ao sistema hematológico.
A compreensão das adaptações hematológicas ao treinamento de endurance e às intervenções artificiais — como altitude simulada e doping sanguíneo — revela um continuum fisiológico no qual as fronteiras entre o natural e o manipulado tornam-se, muitas vezes, tênues. A literatura aponta que os mesmos mecanismos que sustentam a elevação do VO₂máx ao longo de um programa de treinamento — como expansão de volume sanguíneo, aumento de massa de hemoglobina (Hbmass), remodelamento cardíaco e maior capacidade oxidativa muscular — também são o alvo das estratégias de doping, que buscam mimetizar, de forma abrupta e supra-fisiológica, adaptações que o organismo alcança gradualmente.
Dentro desse espectro, observações obtidas em equipes profissionais de ciclismo evidenciam que os marcadores hematológicos são altamente dinâmicos e sensíveis ao contexto competitivo. Durante uma temporada completa, há tendência de queda progressiva da hemoglobina ([Hb]) e do hematócrito (Hct), valores que são consistentemente menores em fases de competição — e especialmente em grandes voltas de três semanas — quando comparados ao período fora de competição. Esse padrão reflete principalmente hemodiluição resultante do aumento de volume plasmático, desgaste provocado por volumes extremos de treinamento e possível hemólise mecânica induzida por esforços prolongados. A recuperação dos níveis basais ocorre apenas após o encerramento da temporada, mostrando que o sistema hematológico acompanha o ciclo de estresse e recuperação imposto pelo calendário competitivo.
Diante dessa oscilação, qualquer tentativa de interpretar um hemograma visando identificar manipulação sanguínea precisa obrigatoriamente considerar o momento da coleta, a carga recente de treino, a fase da temporada e fatores ambientais como altitude. Ignorar essas variáveis constitui um erro metodológico que pode gerar falsos alarmes em programas de controle de doping. É nesse contexto que surge a lógica do passaporte biológico: em vez de buscar apenas substâncias proibidas, monitora-se ao longo do tempo o perfil individual do atleta, observando padrões de variação de Hb, Hct, reticulócitos e índices compostos como o OFF-score. Manifestações incompatíveis com a variabilidade fisiológica esperada — como aumento de Hb acompanhado de queda relativa de reticulócitos — funcionam como assinaturas indiretas de intervenção artificial, refletindo o impacto de uma massa hemoglobínica supra-fisiológica sobre a eritropoiese.
Paralelamente ao avanço das estratégias de detecção, a pesquisa em fisiologia do exercício segue tentando delimitar, com maior precisão, os determinantes centrais e periféricos do aumento do VO₂máx com o treinamento. Evidências demonstram que não existe uma resposta universal; a contribuição relativa de cada componente depende da intensidade, duração e progressão do treino, bem como do estado inicial do indivíduo.
Em intervenções de curta duração, como protocolos de cerca de seis semanas aplicados em indivíduos destreinados, o aumento do VO₂máx — em torno de 9% — acompanha-se principalmente de expansão do volume sanguíneo, aumento de Hbmass e maior débito cardíaco de pico, embora também haja sinais de maior densidade mitocondrial e capilarização muscular. Entretanto, quando o aumento de glóbulos vermelhos é revertido por flebotomia, o ganho de VO₂máx desaparece, mostrando que, nesse horizonte temporal, o motor central é o fator preponderante. As adaptações periféricas, embora presentes, ainda não são suficientes para sustentar o novo patamar de consumo de oxigênio na ausência da expansão hematológica.
Quando o período de treinamento se estende para cerca de dez semanas, observa-se um cenário diferente. O VO₂máx aumenta em torno de 11% tanto em ciclismo ereto quanto em decúbito dorsal, acompanhado por pequenos incrementos em Hbmass, remodelamento cardíaco e marcadores de maior densidade mitocondrial. No entanto, mesmo após a remoção experimental do aumento de Hbmass, o VO₂máx continua elevado. Esse comportamento indica que, com o prolongamento do treinamento, o organismo consolida adaptações centrais — como aumento persistente do débito cardíaco de pico — e periféricas — como maior extração de oxigênio pelo músculo — que tornam o sistema cardiorrespiratório menos dependente de variações transitórias de volume sanguíneo.
Outros cenários reforçam a plasticidade do sistema hematológico. Em ciclistas recreacionais que aumentam expressivamente o volume semanal de treino, observa-se elevação tanto de Hct quanto de [Hb], sem sinais de hemodiluição. Isso sugere um estímulo proporcionalmente maior à eritropoiese do que à expansão plasmática, resultando em sangue relativamente mais concentrado. A interpretação possível é que, nesses indivíduos, o aumento abrupto de quilometragem gera hipóxia tecidual repetida, estresse mecânico e micro-hemólise que sinalizam de modo mais robusto para a produção aumentada de eritrócitos.
A discussão torna-se ainda mais complexa quando se analisam estratégias de altitude simulada, como o modelo “live high – train low” (LHTL). Teoricamente, a exposição prolongada à hipóxia deveria aumentar Hbmass e melhorar o VO₂máx ao nível do mar. Entretanto, resultados mostram que apenas metade dos atletas submetidos a quatro semanas de LHTL apresenta aumentos significativos de Hbmass. E, entre esses respondedores, quando o ganho de hemoglobina é revertido por hemodiluição isovolêmica, o VO₂máx diminui cerca de 6%, demonstrando que o benefício do LHTL, quando presente, é predominantemente hematológico e não periférico. Não se observam alterações marcantes na maquinaria oxidativa muscular, o que reforça que a altitude simulada atua de forma centrada no componente de transporte de oxigênio.
Essas observações convergem com o princípio fisiológico subjacente ao doping sanguíneo: tanto transfusões quanto eritropoetina recombinante têm como objetivo final aumentar de maneira abrupta a Hbmass, ampliando a capacidade de transporte de oxigênio e, com isso, o VO₂máx e o desempenho. Os incrementos observados em laboratório e campo reforçam por que tais manipulações são eficazes — e por que apresentam riscos severos relacionados à hipercoagulação, policitemia e sobrecarga cardiovascular.
Quando esses diversos modelos — temporada de World Tour, intervenções em destreinados, aumentos volumosos de treino em recreacionais e estratégias de hipóxia em atletas treinados — são analisados lado a lado, emerge uma compreensão integrada: o sangue atua como um verdadeiro órgão de interface entre carga de treino, ambiente e resposta adaptativa. Em certos momentos, pequenas flutuações em volume plasmático e Hbmass determinam de forma decisiva o VO₂máx. Em outros, o protagonismo passa ao remodelamento cardíaco, à expansibilidade mitocondrial e à maior densidade capilar periférica. Essa interação, por vezes sutil e multifatorial, torna qualquer interpretação isolada de marcadores hematológicos não apenas imprecisa, mas potencialmente injusta quando aplicada a contextos de controle antidoping.
Assim, compreender a “coreografia” entre adaptações hematológicas, cardiovasculares e musculares é fundamental para o planejamento racional do treinamento, para a interpretação contextualizada de exames laboratoriais e para o desenvolvimento de estratégias antidoping que sejam sensíveis às manipulações artificiais sem criminalizar a fisiologia legítima do esforço humano. Essa visão integrada reforça que o desempenho é sempre um produto da interação entre biologia, carga de treino, ambiente e tempo — e que o sangue, nesse processo, é tanto mensageiro quanto protagonista.
Avaliação hematológica para o treinamento de Endurance
A avaliação hematológica de atletas de endurance exige uma leitura integrada de múltiplos marcadores, uma vez que o treinamento modifica simultaneamente o volume plasmático, a massa eritrocitária, a taxa de renovação das hemácias e a disponibilidade de ferro. A interpretação isolada de parâmetros como hemoglobina ou hematócrito pode levar a conclusões equivocadas, especialmente porque essas variáveis são altamente sensíveis às oscilações do volume plasmático induzidas pelo exercício. Assim, compreender se o treinamento está estimulando a eritropoiese — e, portanto, contribuindo para aumentar a capacidade de transporte de oxigênio — depende de analisar não apenas a concentração de glóbulos vermelhos, mas também os sinais indiretos da atividade da medula óssea, do estado do metabolismo do ferro e da ocorrência de hemólise fisiológica.
Entre os marcadores centrais está a contagem de reticulócitos, que reflete a taxa de produção de hemácias pela medula óssea e responde rapidamente a estímulos como hipóxia funcional, aumento da demanda metabólica e micro-hemólise induzida por exercícios repetitivos. Um discreto aumento de reticulócitos — geralmente dentro da faixa fisiológica — indica que o organismo está elevando a produção eritropoiética, tanto para atender ao aumento da necessidade de transporte de oxigênio quanto para repor hemácias danificadas pelo estresse mecânico. Entretanto, essa variável só adquire significado pleno quando interpretada junto à hemoglobina, hematócrito e contagem total de eritrócitos. Reduções iniciais de hemoglobina e hematócrito, muito comuns durante períodos de grande carga de treino, não representam perda de hemácias, mas sim expansão do volume plasmático. Esse fenômeno, conhecido como hemodiluição, reduz a viscosidade sanguínea, melhora o retorno venoso e facilita o aumento do volume sistólico, sendo uma das adaptações mais benéficas do treino de endurance. Nessa fase, o padrão típico é hemoglobina e hematócrito em queda, reticulócitos levemente elevados e contagem de hemácias relativamente estável.
Outro grupo de marcadores fundamentais é composto pelas variáveis relacionadas ao metabolismo do ferro — ferritina, transferrina, saturação de transferrina e capacidade total de ligação do ferro. A eritropoiese depende fortemente da disponibilidade adequada de ferro, e atletas de endurance frequentemente apresentam redução dos estoques corporais devido à combinação de sudorese, hemólise, perdas gastrointestinais e aumento da demanda medular. A ferritina sérica, nesse contexto, funciona como indicador dos estoques; valores persistentemente baixos podem limitar a resposta eritropoiética, mesmo na presença de estímulos de treinamento. Já a saturação de transferrina e a capacidade total de ligação do ferro (TIBC: Total Iron-Binding Capacity) auxiliam na distinção entre ferropenia absoluta e ferropenia funcional — esta última decorrente de processos inflamatórios associados ao treino intenso, nos quais o ferro fica sequestrado e indisponível para a medula.
Marcadores de hemólise, como haptoglobina e bilirrubina indireta, complementam a interpretação, uma vez que o impacto repetitivo da corrida ou a vibração mecânica do ciclismo podem provocar destruição leve, mas contínua, das hemácias. A queda da haptoglobina e o aumento discreto da bilirrubina sinalizam esse processo, que não é patológico, mas sim parte da fisiologia adaptativa: a hemólise leve atua como estímulo adicional à eritropoiese. Os índices hematimétricos — MCV, MCH e MCHC — também oferecem informações indiretas sobre a dinâmica eritrocitária. Um aumento discreto do MCV, por exemplo, pode indicar maior liberação de reticulócitos, que são células maiores. Já reduções de MCV e MCH sugerem limitação por ferro, interferindo no processo adaptativo.
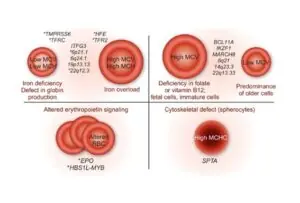
Fonte: Andrews NC. Genes determining blood cell traits. Nat Genet. 2009;41(11):1161-1162.
A compreensão integrada desses parâmetros permite identificar com precisão se o atleta está respondendo fisiologicamente ao treinamento, distinguindo hemodiluição de anemia verdadeira, e separando adaptações legítimas de padrões que exigem intervenção nutricional ou redução momentânea da carga de treino. Também oferece uma base sólida para interpretar dados no contexto do passaporte biológico, no qual padrões de variação — e não valores isolados — são a principal ferramenta para detectar manipulação artificial da eritropoiese. Em suma, o exame hematológico de um atleta treinado deve ser lido como um sistema adaptativo multifatorial, no qual o volume plasmático, o estado do ferro, a produção medular e a integridade das hemácias se entrelaçam para revelar, em conjunto, a história fisiológica da carga de treino recente.
Referências
Mørkeberg JS, Belhage B, Damsgaard R. Changes in blood values in elite cyclist. Int J Sports Med. 2009;30(2):130-138.
Montero D, Cathomen A, Jacobs RA, et al. Haematological rather than skeletal muscle adaptations contribute to the increase in peak oxygen uptake induced by moderate endurance training. J Physiol. 2015;593(20):4677-4688.
Robach P, Siebenmann C, Jacobs RA, et al. The role of haemoglobin mass on VO(2)max following normobaric ‘live high-train low’ in endurance-trained athletes. Br J Sports Med. 2012;46(11):822-827.
Skattebo Ø, Bjerring AW, Auensen M, et al. Blood volume expansion does not explain the increase in peak oxygen uptake induced by 10 weeks of endurance training. Eur J Appl Physiol. 2020;120(5):985-999.
