Evolução da Circulação Humana e Plasticidade Microvascular: da Filogênese às Adaptações ao Exercício
A história da circulação humana é, antes de tudo, a história da própria vida enquanto processo dissipativo. Dos primeiros organismos multicelulares às complexas sociedades contemporâneas, a necessidade de transportar energia, eliminar resíduos e sustentar tecidos metabolicamente exigentes moldou estruturas cuja sofisticação se amplia à medida que as demandas biológicas se tornam mais complexas. A circulação sanguínea representa, nesse sentido, a convergência entre evolução biológica, pressões ambientais e mecanismos adaptativos finamente orquestrados, cujo ápice, em termos de endurance e eficiência hemodinâmica, encontra-se nos humanos modernos.
A microcirculação — essa vasta rede de capilares que se estende silenciosamente por todos os órgãos — emerge como o palco onde forma, função e adaptação se encontram e se expressam. É nela que se decidem a troca gasosa, o metabolismo de nitrogênio, o controle vasomotor, a redistribuição do fluxo durante o exercício e a própria sobrevivência celular. Compreender como a microvasculatura alcançou tamanho desempenho requer, portanto, voltar aos princípios evolutivos e seguir o fluxo do sangue através da história filogenética, para então examinar como o exercício, essa força ancestral e cotidiana, continua a remodelar dinamicamente o sistema vascular humano.
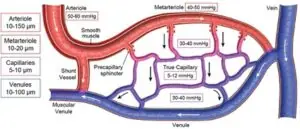
Fonte: Cooper ES, Silverstein DC. Fluid Therapy and the Microcirculation in Health and Critical Illness. Front Vet Sci. 2021;8:625708.
Do ponto de vista evolutivo, a circulação é um testemunho de soluções sucessivas para desafios progressivamente mais complexos. Evidencias mostram que a transição dos peixes para os vertebrados terrestres envolveu ajustes fundamentais na homeostase interna, sobretudo graças ao desenvolvimento do rim e ao estabelecimento do que chamam de “oceano interior” — um ambiente iônico estável que permitiu aos organismos suportar as flutuações ambientais externas e, posteriormente, o avanço para a terra firme.
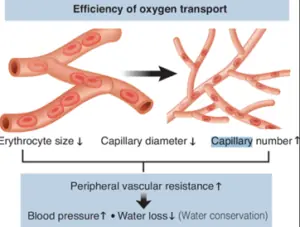
Fonte: Nishiyama A, Kitada K, Suzuki M. Blood pressure adaptation in vertebrates: comparative biology. Kidney Int. 2022;102(2):242-247.
O salto evolutivo subsequente — a separação entre circulação pulmonar e sistêmica — transformou a dinâmica hemodinâmica dos animais, permitindo pressões sistêmicas mais altas sem comprometer a delicadeza dos capilares pulmonares. Esse rearranjo anatômico e funcional, observado tanto em aves quanto em mamíferos, abriu espaço para um aumento extraordinário da taxa metabólica, propiciando níveis inéditos de performance física. Complementarmente, outras análises revelam que os corações evoluíram de tubos peristálticos lentos e abertos, característicos de invertebrados, até sistemas fechados e altamente pressurizados, com quatro câmaras independentes, capazes de manter fluxo estável, pulsátil e eficiente através de vastas redes microcapilares.
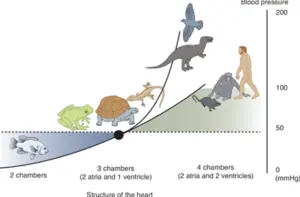
Fonte Nishiyama A, Kitada K, Suzuki M. Blood pressure adaptation in vertebrates: comparative biology. Kidney Int. 2022;102(2):242-247.
O advento do ventrículo duplo não apenas refinou a entrega de oxigênio, como permitiu que a microcirculação se tornasse incrivelmente densa, regulada e responsiva, especialmente em mamíferos endotérmicos. Essa trajetória evolutiva, porém, não se apoia exclusivamente na mudança de estruturas anatômicas. A forma e a função dos organismos emergem de processos dissipativos, nos quais células e tecidos se organizam de modo a otimizar a extração e o uso de energia do ambiente, obedecendo ao princípio de menor ação e à segunda lei da termodinâmica.
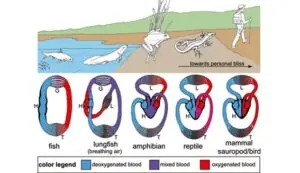
Fonte: Schulte K, Kunter U, Moeller MJ. The evolution of blood pressure and the rise of mankind. Nephrol Dial Transplant. 2015;30(5):713-723.
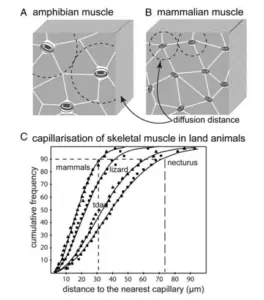
A microcirculação, ao maximizar a superfície de troca por unidade de volume e ao minimizar o custo energético para difusão, é exemplo paradigmático desse tipo de solução emergente. Ela se desenvolve não apenas como resposta genética, mas como fenômeno físico-organizado, no qual a pressão, a resistência e o fluxo se ajustam a demandas locais e globais, permitindo ao organismo alcançar níveis inéditos de complexidade.
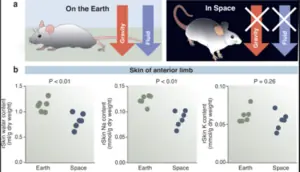
Fonte: Nishiyama A, Kitada K, Suzuki M. Blood pressure adaptation in vertebrates: comparative biology. Kidney Int. 2022;102(2):242-247.
Esse cenário evolutivo pavimentou o caminho para uma microcirculação altamente responsiva às condições funcionais, mas é o exercício que, na contemporaneidade, representa o estímulo mais poderoso para remodelar a vasculatura humana. O exercício físico, ao aumentar dramaticamente o fluxo sanguíneo muscular, eleva o estresse de cisalhamento — a força tangencial exercida pelo fluxo sobre o endotélio — e desencadeia uma cascata de sinais celulares que modulam a biodisponibilidade de óxido nítrico (NO), remodelam a estrutura arterial e ajustam a densidade capilar. A revisão monumental de Green e colaboradores mostra que as forças hemodinâmicas associadas ao exercício — cisalhamento, pressão pulsátil, distensão cíclica e tensão de parede — constituem estímulos mecanotransdutores capazes de gerar adaptações funcionais e estruturais robustas na rede vascular humana, independentemente de mudanças nos fatores de risco tradicionais.
Fonte: Schulte K, Kunter U, Moeller MJ. The evolution of blood pressure and the rise of mankind. Nephrol Dial Transplant. 2015;30(5):713-723.
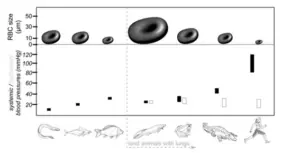
De modo notável, o exercício melhora a função endotelial, promove angiogênese, aumenta o diâmetro arterial em segmentos específicos e reduz a espessura da parede vascular, contribuindo para um sistema capaz de acomodar maiores volumes de fluxo com menor custo energético e maior eficiência de distribuição. Essa compreensão se aprofunda com os achados experimentais de Casey et al., que demonstram que mesmo exercícios leves são capazes de aumentar substancialmente a fosforilação da eNOS em humanos, sem alterar o conteúdo total da enzima. Esse detalhe é crucial: a resposta adaptativa inicial do endotélio ao exercício ocorre em minutos e depende de modificações pós-traducionais, tornando a microcirculação um tecido extremamente plástico, sensível ao ambiente hemodinâmico e capaz de ajustes rápidos e precisos na vasodilatação dependente de NO.
Fonte: Schulte K, Kunter U, Moeller MJ. The evolution of blood pressure and the rise of mankind. Nephrol Dial Transplant. 2015;30(5):713-723.
São adaptações instantâneas, que preparam o organismo para esforços repetidos, sustentam o fluxo capilar e otimizam a troca metabólica. As adaptações estruturais mais duradouras, por sua vez, emergem do uso crônico da circulação sob demanda. Atletas de elite frequentemente exibem artérias de maior calibre e paredes mais finas, fenômeno que, paradoxalmente, reduz a resposta relativa de dilatação — o FMD — mesmo quando sua função microvascular é superior à de indivíduos sedentários. O estudo de Green et al. (2013) ilustra esse aparente paradoxo ao mostrar que um menor FMD em atletas não indica disfunção, mas sim uma reconfiguração estrutural: artérias maiores dilatam proporcionalmente menos porque já operam em um estado de adaptação estrutural avançada induzida pelo exercício contínuo.
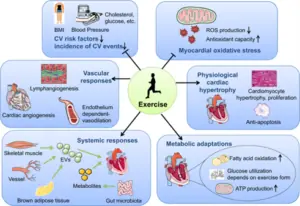
Fonte: Chen H, Chen C, Spanos M, et al. Exercise training maintains cardiovascular health: signaling pathways involved and potential therapeutics. Signal Transduct Target Ther. 2022;7(1):306.
A microcirculação nesse contexto encontra-se ampliada, com maior densidade capilar e melhora da perfusão tecidual — fatores essenciais para o transporte de oxigênio durante esforços prolongados. Além disso, o impacto das adaptações vasculares deve ser apreciado à luz das diferenças sexuais e metodológicas. A revisão sistemática de Thompson e colegas revela que, apesar do crescente interesse na fisiologia feminina, persistem lacunas significativas no controle das variáveis hormonais e na representatividade de mulheres em estudos de FMD e exercício, o que limita conclusões amplas sobre as diferenças sexuais na função microvascular adaptativa
Como a sensibilidade endotelial ao estrogênio e às oscilações do ciclo menstrual é alta, a microcirculação feminina talvez apresente padrões distintos de plasticidade e regulação hemodinâmica — uma área de pesquisa que permanece em expansão. Finalmente, mesmo estudos aparentemente distantes da hemodinâmica, como o de Singer sobre estratégias de conservação de nitrogênio em vertebrados, reforçam o papel integrador da microcirculação na homeostase sistêmica. O transporte de ureia, amônia e aminoácidos depende profundamente do fluxo capilar e da dinâmica entre tecidos, microbiota intestinal e rim, concluindo que o metabolismo, a circulação e o ambiente interno são interdependentes em graus muito profundos.
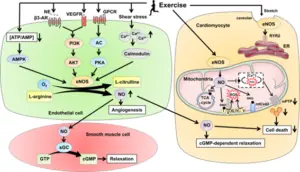
Fonte: Chen H, Chen C, Spanos M, et al. Exercise training maintains cardiovascular health: signaling pathways involved and potential therapeutics. Signal Transduct Target Ther. 2022;7(1):306.
Em conjunto, esses estudos revelam que a microcirculação é tanto produto quanto protagonista da história evolutiva e funcional do organismo humano. Ela condensa pressões seletivas ancestrais, princípios físicos universais e uma impressionante capacidade adaptativa que se intensifica com a prática regular de exercício. A evolução lhe deu forma; o exercício lhe dá movimento. E é justamente na interação entre esses dois eixos — filogênese e experiência funcional — que se delineia a singularidade do sistema vascular humano, capaz de suportar desde a corrida persistente dos caçadores do deserto até o esforço extremo dos atletas contemporâneos. Assim, ao seguir o caminho do sangue pelos vastos corredores microscópicos que atravessam o corpo, percebemos que a microcirculação é mais do que um mecanismo fisiológico: é uma resposta biológica sofisticada, moldada ao longo de milhões de anos e continuamente redesenhada pelo modo como vivemos, nos movemos e nos adaptamos.
Referências:
Baverstock K, Rönkkö M. The evolutionary origin of form and function. J Physiol. 2014;592(11):2261-2265.
Bettex DA, Prêtre R, Chassot PG. Is our heart a well-designed pump? The heart along animal evolution. Eur Heart J. 2014;35(34):2322-2332.
Casey DP, Ueda K, Wegman-Points L, Pierce GL. Muscle contraction induced arterial shear stress increases endothelial nitric oxide synthase phosphorylation in humans. Am J Physiol Heart Circ Physiol. 2017;313(4):H854-H859.
Green DJ, Hopman MT, Padilla J, Laughlin MH, Thijssen DH. Vascular Adaptation to Exercise in Humans: Role of Hemodynamic Stimuli. Physiol Rev. 2017;97(2):495-528.
Green DJ, Rowley N, Spence A, et al. Why isn’t flow-mediated dilation enhanced in athletes?. Med Sci Sports Exerc. 2013;45(1):75-82.
Schulte K, Kunter U, Moeller MJ. The evolution of blood pressure and the rise of mankind. Nephrol Dial Transplant. 2015;30(5):713-723.
Singer MA. Do mammals, birds, reptiles and fish have similar nitrogen conserving systems?. Comp Biochem Physiol B Biochem Mol Biol. 2003;134(4):543-558.
Thompson SL, Brade CJ, Henley-Martin SR, Naylor LH, Spence AL. Vascular adaptation to exercise: a systematic review and audit of female representation. Am J Physiol Heart Circ Physiol. 2024;326(4):H971-H985.
