A microcirculação humana é um continente microscópico onde a vida se decide em escalas diminutas, mas com consequências imensas. É nesse território composto por arteríolas, capilares, vênulas e pelo delicado epitélio endotelial que o organismo negocia permanentemente o abastecimento de oxigênio, a remoção de resíduos metabólicos, o equilíbrio térmico, a vigilância imune e até a arquitetura da reparação tecidual. Embora represente apenas cerca de 7% do volume sanguíneo total, essa rede organiza-se em padrões fractais, como descreve Gutterman, replicando curvas, ramificações e proporções que garantem que nenhuma célula do corpo permaneça distante da fonte que a sustenta. É uma obra de engenharia viva onde a geometria serve à fisiologia e onde o acesso ao oxigênio — a moeda energética da existência — é minuciosamente orquestrado.
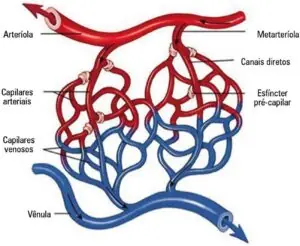
Fonte: Tafner PFDA, Chen FK, Rabello R Filho, Corrêa TD, Chaves RCF, Serpa A Neto. Recent advances in bedside microcirculation assessment in critically ill patients. Rev Bras Ter Intensiva. 2017 Apr-Jun;29(2):238-247.
Essa complexa rede não funciona como um simples duto; ela pensa, interpreta e responde. Cada porção do microvaso é um espaço de tomada de decisão hemodinâmica. A arteríola terminal regula o fluxo com sensibilidade quase nervosa; o capilar, com seu revestimento unicelular, cria a superfície através da qual moléculas e sinais atravessam; as vênulas, por sua vez, acolhem, drenam e também sinalizam. O glicocálice endotelial paira sobre essa estrutura como um véu bioquímico vibrátil: é barreira, sensor, tradutor de forças de cisalhamento e estrutura antiflogística. Quando este delicado tapete de proteoglicanos e glicoproteínas se rompe, seja por inflamação, hiperglicemia ou trauma circulatório, a permeabilidade se altera, a adesão leucocitária aumenta e os alicerces silenciosos da homeostase começam a ruir — evidência clara de que a microcirculação é o primeiro lugar onde a doença se manifesta, muitas vezes antes que a macrocirculação denuncie qualquer alteração perceptível.
Fonte: Tafner PFDA, Chen FK, Rabello R Filho, Corrêa TD, Chaves RCF, Serpa A Neto. Recent advances in bedside microcirculation assessment in critically ill patients. Rev Bras Ter Intensiva. 2017 Apr-Jun;29(2):238-247.
A função microvascular nasce da combinação engenhosa entre controle sistêmico e regulação local. Hormônios, nervos simpáticos, mediadores inflamatórios e forças mecânicas modulam sistemicamente o tônus vascular; ao mesmo tempo, o próprio tecido comunica-se com o microvaso através de gradientes metabólicos de oxigênio, dióxido de carbono, adenosina, ácido lático e inúmeros outros sinais bioenergéticos. O endotélio, longe de ser mero intermediário, torna-se um maestro bioquímico capaz de liberar óxido nítrico, prostaglandinas e outros efetores vasodilatadores que protegem o parênquima, preservam a função mitocondrial e mantêm a circulação em um estado de vigilância flexível. Gutterman descreve esse fenômeno como acoplamento vásculo-parenquimal, um conceito que revela que o microvaso e a célula tecidual não são parceiros distantes, mas sim sistemas entrelaçados, cujas funções convergem para garantir equilíbrio, fluxo e sobrevivência. Quando o estresse oxidativo predomina, a microcirculação muda de natureza: o NO cede lugar às espécies reativas de oxigênio como mediadores principais, e aquilo que era sincronização transforma-se em disritmia inflamatória, pró-trombótica e disfuncional.
Mas é na entrega final do oxigênio ao tecido muscular que a microcirculação revela uma beleza quase dramática. Durante décadas imaginou-se um gradiente suave e progressivo entre o capilar e as mitocôndrias. Descobertas recentes, porém, mostram que esse percurso é marcado por quedas abruptas de pressão parcial de oxigênio, especialmente na finíssima distância que separa o eritrócito da membrana endotelial. Pesquisadores como Poole demonstram que este pequeno percurso — inferior a cinquenta micrômetros — é, paradoxalmente, o grande gargalo fisiológico do transporte de oxigênio. O oxigênio precisa atravessar membranas, dissolver-se brevemente no plasma, cruzar o glicocálice, penetrar o endotélio, alcançar o interstício, entrar na fibra muscular e, finalmente, alcançar as mitocôndrias, que hoje são compreendidas menos como organelas isoladas e mais como redes contínuas, de plasticidade dinâmica, capazes de transmitir energia e até facilitar o transporte molecular. Nesse cenário revisado, a microcirculação não é apenas condutora: ela é coautora da respiração celular.
No músculo esquelético, essa trama adquire nuances ainda mais sofisticadas. A microcirculação não só entrega oxigênio e glicose; ela determina a própria biologia da fibra muscular. Pepe e Albrecht mostram que células endoteliais e células satélites dialogam de maneira fina, influenciando a regeneração muscular, a angiogênese e até a sensibilidade à insulina. Cada capilar funciona como tutor metabólico da fibra à qual se associa. Em estados como diabetes e hipertensão, a ruptura desse diálogo inaugura o cenário clássico da resistência insulínica, em que a capilarização diminuída e a vasodilatação prejudicada limitam o acesso da insulina à fibra, rompendo o eixo vascular-metabólico.
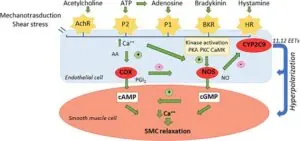
Fonte: De Ciuceis C, Rizzoni D, Palatini P. Microcirculation and Physical Exercise In Hypertension. Hypertension. 2023;80(4):730-739.
A microcirculação sofre de maneira particularmente intensa nos estados críticos. Na sepse, na hemorragia ou no trauma, ela perde sua coerência interna, produzindo heterogeneidade perfusional extrema, shunts funcionais e dissociação entre macrocirculação e oxigenação tecidual. Pode-se observar pressão arterial normal enquanto o tecido afoga-se em hipóxia. Isso ocorre porque o glicocálice se degrada, o endotélio inflama, a vasorreatividade se perde e a mitocôndria passa a operar de maneira irregular. Como descrevem Cooper e Silverstein, a avaliação microvascular torna-se a chave clínica para entender por que algumas terapias aparentemente eficazes ao nível sistêmico não restauram a vitalidade celular.
Nesse panorama, o exercício físico emerge não como adjuvante, mas como estímulo de primeira grandeza. Li e colaboradores mostram que o exercício é capaz de aumentar a densidade capilar, aprimorar a função endotelial, reduzir inflamação, melhorar o estresse oxidativo, ampliar a biodisponibilidade de NO e reconfigurar a microcirculação em um estado mais resiliente. Green e Smith reforçam que o exercício age diretamente sobre a parede vascular por meio do cisalhamento repetido, remodelando-a em direção a um fenótipo antiaterogênico, responsivo e mais apto a manter o equilíbrio perfusional. Do ponto de vista evolutivo, o exercício não é um luxo metabólico, mas uma necessidade biológica que mantém viva a maquinaria microvascular.
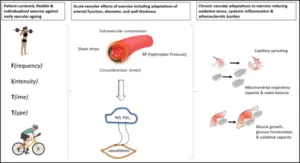
Fonte: Königstein K, Dipla K, Zafeiridis A. Training the Vessels: Molecular and Clinical Effects of Exercise on Vascular Health-A Narrative Review. Cells. 2023;12(21):2544.
A cada novo estímulo mecânico que atravessa a parede vascular durante o exercício, o endotélio parece recordar sua vocação primordial: ler o fluxo, traduzir força em linguagem bioquímica e responder como um organismo que busca equilíbrio. É nesse diálogo íntimo entre sangue em movimento, e células que se renovam, que entram em cena os mecanismos de adaptação mais finos. O aumento do shear stress deforma sensores do glicocálix e desperta canais de cálcio, inaugurando uma cascata que libera prostaglandinas, ativa a fosforilação da eNOS e amplia o pulso de óxido nítrico. A musculatura lisa adjacente, ao receber esse sinal, afrouxa a rigidez tônica e permite que a luz arterial se abra como quem solta um suspiro de rendição fisiológica. É uma coreografia que, embora escondida aos olhos, sustenta o ritmo das nossas capacidades mais humanas: mover-se, resistir, adaptar-se.
Com o tempo, esses episódios repetidos deixam de ser apenas respostas agudas e começam a esculpir o tecido vascular. A parede do vaso aprende com a insistência do fluxo. Angiogênese e arteriogênese irrompem como pequenas obras de arquitetura viva: novos capilares brotam, arteríolas se expandem, e a densidade microvascular cresce em fibras lentas e rápidas, cada uma modulada pela história metabólica do músculo que alimentam. A cada semana de prática consistente, o mapa da circulação periférica se multiplica em ramificações mais finas, como se o organismo, movido pela repetição voluntária do gesto atlético, se reinventasse para carregar oxigênio com mais generosidade. Essas adaptações estruturais não surgem em dias, mas em semanas e meses, compondo uma lenta poesia tecidual que amplia a reserva vasodilatadora e melhora a entrega de oxigênio.
Ao mesmo tempo, o “treinamento dos vasos” ultrapassa o domínio estrutural e avança para dimensões funcionais e celulares que sustentam o fenômeno. A maquinaria mitocondrial das células musculares lisas — discreta, pequena em volume, mas decisiva — responde ao exercício com uma renovação impressionante. A biogênese mitocondrial se intensifica, a fusão e a fissão se equilibram como movimentos de lapidação interna, e a mitofagia garante que organelas danificadas não comprometam a eficiência redox. Com isso, o ambiente intravascular torna-se menos vulnerável ao estresse oxidativo crônico, e o tónus vasomotor se ajusta de maneira mais precisa. Paradoxalmente, o mesmo exercício que induz ROS agudamente é o que reduz a carga oxidativa quando praticado de forma crônica. A repetição ordenada, portanto, não apenas fortalece a estrutura, mas refina o metabolismo interno das células vasculares.
Esse refinamento fisiológico encontra eco nas evidências clínicas. Populações ativas mostram menor rigidez arterial, maior responsividade endotelial e menor progressão da disfunção microvascular ao longo das décadas. Mesmo quando fatores de risco coexistem — hipertensão, resistência insulínica, inflamação — o endotélio ainda demonstra notável plasticidade frente ao estímulo físico regular. A vasculatura envelhece, claro, mas envelhece de forma mais tardia, preservando o diálogo molecular que sustenta o fluxo. O exercício não apenas “evita doença”; ele reorganiza a maneira como o corpo interpreta e responde às pressões internas da vida cotidiana. Funciona como uma educação contínua do tecido vascular, ensinando-o a reagir com flexibilidade e economia energética.
No nível prático, a literatura mostra que não é o pico de intensidade que molda os vasos, mas a soma reiterada dos estímulos. Sessões moderadas, longas o bastante para elevar de forma sustentada o shear stress, parecem provocar adaptações mais robustas do que explosões intensas, embora estas também carreguem benefícios metabólicos importantes. A vasculatura responde menos ao espetáculo agudo e mais ao hábito: intensidade moderada, repetição quase cotidiana, variações planejadas ao longo da semana e o casamento de exercícios aeróbicos e resistidos. Cada modalidade imprime no vaso uma assinatura distinta — ora ampliando o lume, ora modulando a complacência, ora ajustando a microcirculação — e juntas compõem um mosaico de estímulos que mantém a saúde vascular em sua forma mais completa.
Assim, ao treinar os músculos, treinam-se também os corredores invisíveis que os alimentam. O exercício físico, visto por essa lente, transforma-se em um artesanato interno lento e constante. Cada caminhada, pedalada ou corrida redesenha o comportamento do endotélio; cada repetição de força ensina o vaso a resistir sem endurecer; cada sessão renovada reforça a parceria entre fluxo e parede. No fim, “treinar os vasos” não é metáfora, mas literalidade fisiológica: o corpo, exposto ao movimento regular, aprende a circular melhor, iluminar melhor seus tecidos, e sustentar-se com mais vigor ao longo da vida.
Assim, a microcirculação humana não deve ser entendida como simples rede de tubos microscópicos, mas como uma ecologia viva, onde fluido, sinalização, metabolismo e estrutura se condensam em uma coreografia contínua. Através dela o organismo interpreta necessidades, antecipa riscos e molda respostas. É o teatro íntimo onde o oxigênio se converte em energia, onde a inflamação nasce ou se resolve, onde o movimento se inicia, onde a vida pulsa em escala imperceptível. Quem observa a microcirculação testemunha a própria lógica da fisiologia: um diálogo constante entre fluxo e forma, entre limite e adaptação, entre fragilidade e potência. É ali, no sopro das pequenas correntes, que o corpo negocia sua permanência no mundo.
Referências:
Cooper ES, Silverstein DC. Fluid Therapy and the Microcirculation in Health and Critical Illness. Front Vet Sci. 2021;8:625708.
Green DJ, Smith KJ. Effects of Exercise on Vascular Function, Structure, and Health in Humans. Cold Spring Harb Perspect Med. 2018 Apr 2;8(4):a029819.
Gutterman DD, Chabowski DS, Kadlec AO, et al. The Human Microcirculation: Regulation of Flow and Beyond. Circ Res. 2016;118(1):157-172.
Königstein K, Dipla K, Zafeiridis A. Training the Vessels: Molecular and Clinical Effects of Exercise on Vascular Health-A Narrative Review. Cells. 2023;12(21):2544.
Li J, Liu G, Zhang D, Zhang K, Cao C. Physiological Mechanisms Driving Microcirculatory Enhancement: the Impact of Physical Activity. Rev Cardiovasc Med. 2025 Feb 19;26(2):25302.
Pepe GJ, Albrecht ED. Microvascular Skeletal-Muscle Crosstalk in Health and Disease. Int J Mol Sci. 2023;24(13):10425.
Poole DC, Behnke BJ, Padilla DJ. Dynamics of muscle microcirculatory oxygen exchange. Med Sci Sports Exerc. 2005;37(9):1559-1566.
Poole DC, Musch TI, Colburn TD. Oxygen flux from capillary to mitochondria: integration of contemporary discoveries. Eur J Appl Physiol. 2022;122(1):7-28.
Wang G, Lian H, Zhang H, Wang X. Microcirculation and Mitochondria: The Critical Unit. J Clin Med. 2023;12(20):6453.
